Neurodegenerativní onemocnění
Transkript
Neurodegenerativní onemocnění Od molekulární genetiky k léčbě JIŘÍ HORÁČEK LUCIE MOTLOVÁ Při neurodegenerativních onemocněních postupně zanikají některé populace nervových buněk, což je spojeno s velmi vážnými psychickými a neurologickými příznaky. Ty psychické se projevují ztrátou paměti a rozumových schopností, poruchami chování, často i halucinacemi, bludy a celkovým úpadkem osobnosti, neurologické se týkají především správné koordinace a řízení pohybu a řeči. Jde o vážná onemocnění, která znamenají velkou zátěž pro pacienty, jejich rodiny i společnost. Častým neurodegenerativním onemocněním je Alzheimerova choroba, která postihuje 5–10 % osob starších 65 let. V nejlehčí formě se projevuje zhoršením paměti, ale vede až k naprosté zmatenosti a ztrátě většiny rozumových schopností. Parkinsonova nemoc na sebe upozorní třesem, svalovou ztuhlostí a omezením hybnosti, ale může mít i řadu psychických příznaků. Do této skupiny nemocí patří také Huntingtonova chorea, Jakobova-Creutzfeldtova choroba, různé ataxie a řada dalších. Příčiny a patofyziologie neurodegenerativních onemocnění jsou doposud málo známé. Možnosti léčení jsou nedostatečné, prognóza většiny onemocnění zůstává špatná. Přesto lze mluvit o určitém pokroku. Naději vzbudil výzkum zaměřený na lepší pochopení biologické a genetické podstaty onemocnění a zdá se, že směřuje k efektivnějším léčebným postupům. Rozvoj a genetika neurodegenerativních onemocnění Předpokládáme, že příčinou neurodegenerativního onemocnění je genetická abnormalita, která vyvolá bioPLODNÁ OBDOBÍ VÝZKUMU NEURODEGENERATIVNÍCH ONEMOCNĚNÍ n Počátek tohoto století. Rozvoj mikroskopie a histopatologie umožnil důkladný morfologický výzkum nervové tkáně, který společně s klinickými pozorováními vedl ke klasifikacím platícím dodnes. Tato éra je spojena se jmény velkých neuropatologů a neuropsychiatrů (často v jedné osobně), jako byli Alois Alzheimer, James Parkinson, George S. Huntington, Samuel A. K. Wilson, Arnold Pick, Franz Nissl, Nikolaus Friedreich a další. Jména těchto mužů přežívají v medicínské terminologii (viz tabulku na s. 330–331). Revoluční spojení klinického pohledu s nálezem patologa má ovšem jeden nedostatek. Patolog může stanovit diagnózu až po smrti pacienta, kdežto klinikové se potýkají s časnými stadii nemocí. Časná a pozdní stadia neurodegenerativních nemocí se však mohou výrazně lišit. n Současná doba. Máme k dispozici převratné technologie molekulární genetiky, modely transgenních myší, dokonalejší histologické postupy a zobrazovací metody, které podávají přesný obraz živé nervové tkáně. Funkčně zobrazovacími metodami můžeme dokonce studovat metabolizmus jednotlivých oddílů živého bdělého mozku. Snažíme se výsledky všech těchto přístupů kombinovat, abychom porozuměli onemocnění v celém jeho průběhu a postupu. tab. I chemickou poruchu. Jde buď o omezení produkce některé potřebné bílkoviny, nebo o modifikaci její struktury, která je biologicky nepoužitelná. Buňka může produkovat i bílkovinu, která je vysloveně toxická. Porucha metabolizmu buňky vede k morfologickým odchylkám (např. k atrofii určitých oblastí mozku), a především ke ztrátě funkcí poškozených populací neuronů. Z lokalizace a míry poškození potom vyplývají klinické příznaky. Rozvoj neurodegenerativních onemocnění lze shrnout do jednoduchého schématu (viz tab. I). Většina neurodegenerativních onemocnění je dědičná, ale dědičnost nehraje u všech stejně významnou roli. U Huntingtonovy choroby je velmi významná, u Parkinsonovy nemoci se zase uplatňuje málo. Mutace buď zasáhne jeden gen, nebo změní delší úsek DNA, čímž jsou ovlivněny i geny sousední. Navíc mohou být u jediné choroby mutace několika genů na různých chromozomech. To je typické pro Alzheimerovu demenci (popisovány jsou mutace na chromozomech 21, 19, 14 a 1). Některé nemoci jsou způsobeny priony (viz Vesmír 77, 15, 1998/1). Z typu a lokalizace mutace nelze zcela odvodit konkrétní příznaky nemoci. Abnormality na několika různých genech mohou mít podobné klinické syndromy (například u ataxií). A naopak jedna mutace může vyvolat příznaky značně rozmanité (u prionových onemocnění a demencí). Tento jev se nazývá fenotypová variabilita. Až na výjimky nám pro ni chybí vysvětlení. Dělení neurodegenerativních onemocnění Podle biochemických důsledků genetické mutace je možné většinu neurodegenerativních nemocí rozdělit do dvou hlavních skupin: 1) polyglutaminová onemocnění, 2) taupatie a alfa-synukleinopatie (Science 282, 1075–1079, 1988). Stranou stojí např. familiární amyotrofická laterální skleróza a Wilsonova choroba. Tato nová klasifikace je důležitým výsledkem moderního integrovaného výzkumu. n Polyglutaminová onemocnění. Jedním z největších objevů lidské genetiky je objev mutací, při kterých se patologicky zvýší počet sekvencí určitých tripletů v jednom genu. Hovoříme o expanzi trinukleotidových repetitivních sekvencí. Opakující se triplet cytozin-adenin-guanin (CAG) způsobuje při transkripci patologické zvýšení aminokyseliny glutaminu v kódovaném proteinu. V jádrech neuronů se hromadí polyglutaminové útvary (inkluze) a vedou k porušení jejich funkce. Z lokalizace poškození v nervovém systému můžeme MUDr. Jiří Horáček (*1966) vystudoval Lékařskou fakultu UK v Plzni. V Psychiatrickém centru Praha se zabývá studiem role serotoninu v patofyziologii deprese a problematikou neurokognitivních funkcí u schizofrenie. MUDr. Lucie Motlová (*1965) vystudovala Fakultu všeobecného lékařství v Praze. Přednáší na 3. Lékařské fakultě UK, působí v Psychiatrickém centru Praha. Zabývá se zejména schizofrenií. http://www.cts.cuni.cz/vesmir l VESMÍR 78, červen 1999 307 do jisté míry odvodit i klinické příznaky. Expanze tripletu CAG se podílí na rozvoji několika neurodegenerativních onemocnění, především Huntingtonovy choroby. Gen pro Huntingtonovu chorobu byl objeven na krátkém raménku 4. chromozomu. Na 5' konci obsahuje nestabilní expandovanou repetici CAG. Za normálního stavu se v této oblasti vyskytuje 6 až 37 repetic CAG, u nemocných Huntingtonovou chorobou je jich však daleko více (40 až 121). Čím více je repetic CAG, tím dříve onemocnění začíná. Gen se přenáší na potomky, a navíc se při meióze sekvence repetic CAG dále prodlužuje. Důsledkem této nestability je postižení potomků v nižším věku. Kromě Huntingtonovy choroby patří k polyglutaminovým onemocněním také spinobulbární1) svalová atrofie, některé typy spinocerebelárních2) ataxií ad. Při pokroku molekulární biologie dnes rozumíme, proč bylo v minulosti obtížné některé choroby odlišit. Podobné mutace na různých genech mohou totiž vytvářet podobné klinické obrazy. Laboratorní identifikace repetitivních sekvencí CAG dnes pomáhá přesněji určit diagnózu a v budoucnu asi umožní i specifické terapeutické přístupy. n Taupatie a synukleinopatie. Druhá skupina neurodegenerativních onemocnění je spojena s hromaděním dvou patologických proteinů: jednak proteinu tau, který vytváří v neuronu jakýsi smotek, jednak proteinu alfa-synukleinu, který vytváří v těle neuronů Lewyho tělíska. Hromadění proteinu tau je charakteristické pro demenci u Parkinsonovy choroby, Alzheimerovu chorobu, progresivní supranukleární obrnu, nemoc Guam a některé formy prionových onemocnění. Lewyho tělíska nalézáme u Parkinsonovy choroby, některých forem Alzheimerovy choroby, některých prionových infekcí a u určitého typu demence. Molekulární genetika nyní pomáhá řešit nejasný vztah mezi diagnózou a přítomností té které inkluze. Zdá se, že protein tau a alfa-synuklein se mohou vyskytnout i sekundárně jako důsledek jiného biochemického procesu. U familiárního typu Alzheimerovy choroby (asi 10 % onemocnění) se vyskytuje mutace v genu pro prekurzorový protein beta-amyloid, a to buď presenilin 1, nebo presenilin 2 (geny na chromozomech 21, 14, popřípadě 1). Mutace vedou k produkci peptidu betaamyloidu, který se hromadí v mozku ve formě plaků. Kromě nahromaděného beta-amyloidu však uvnitř neuronu vždy nacházíme smotek proteinu tau a někdy také Lewyho tělíska. Snad jde o reakci cytoskeletonu neuronů na chronický stres. Na druhé straně primární mutace v proteinu tau vede k frontotemporální 3) demenci a mutace v alfa-synukleinu vede ke vzniku Lewyho tělísek u Parkinsonovy nemoci. Dosud není jasné, zda jsou oba mechanizmy reparační reakcí neuronu, nebo zda jsou známkami pomalého umírání buněk. V každém případě jsou mezistupněm mezi normálním a mrtvým neuronem. Vztah příznaku a lokalizace poškození Jednotlivá neurodegenerativní onemocnění postihují určité skupiny neuronů v různých částech nervového systému, proto mluvíme o selektivnosti poškození (selektivní vulnerabilitě). Dnes většinou víme, které fyziologické funkce jsou s těmito strukturami nervového systému spojeny. Z lokalizace poškození v nervovém systému je tedy možné porozumět konkrétním příznakům neurodegenerativních onemocnění. Huntingtonova chorea je způsobena smrtí neuronů v jádře nucleus caudatus, které se podílejí na řízení a koordinaci pohybu. Jejich degenerace vede k chaotickým pohybům vzdáleně připomínajícím tanec (proto chorea). Parkinsonova choroba vzniká v důsledku 1) spinobulbární – týkající se páteřní a prodloužené míchy 2) spinocerebelární – týkající se mozečku a míchy 3) frontotemporální – týkající se oblasti čelní a spánkové 308 VESMÍR 78, červen 1999 l http://www.cts.cuni.cz/vesmir destrukce neuronů v další struktuře bazálních ganglií, která se nazývá substantia nigra a je důležitá pro zahájení volního pohybu. Degenerace této struktury vede k svalové ztuhlosti, třesu a omezení hybnosti. Amyotrofická laterální skleróza postihuje velké motoneurony, důležitou součást motorické dráhy, a vede tedy k slabosti a křečovitému napětí svalstva. Alzheimerova choroba postihuje nejen šedou kůru, ale i hipokampus, který se podílí na mechanizmech paměti. Alzheimerova demence proto vede ke ztrátě paměti a rozumových funkcí. Zjednodušeně lze říci, že zatímco polyglutaminová onemocnění mají tendenci poškozovat mozeček a vedou k postojovým nestabilitám (ataxiím), alfa-synukleinopatie působí poruchu substantia nigra (černošedé hmoty ve středním mozku) a taupatie narušují pyramidové neurony kůry mozkové (projevují se jako demence). Situace je však často mnohem komplikovanější a u značné části nemocných zjišťujeme i docela jiné příznaky, než bychom očekávali podle toho, které neurony byly poraněny. Například v pozdějších stadiích Huntingtonovy choroby, Parkinsonovy choroby a amyotrofické laterální sklerózy se často rozvíjí demence, která je důsledkem poruchy korových neuronů. Alzheimerova nemoc naopak zase může být spojena s příznaky parkinsonizmu. Selektivnost poškození tedy není absolutní, ale je výsledkem spolupůsobení dvou mechanizmů. Chorobný proces napadá určitou skupinu neuronů a stupeň postižení je závislý na čase. Na druhé straně nervový systém vykazuje velkou přizpůsobivost a je schopen dlouho postižení kompenzovat. Příznaky Parkinsonovy nemoci se objeví teprve po destrukci 70 % neuronů v substantia nigra. Katastrofické selhání funkce se projeví až po „překročení hranice“. Nejde o náhlé selhání jedné kvality, narušení je globální a nemoc se začíná projevovat postupně. Jemné a nespecifické projevy lze pozorovat již dlouho před nástupem prvních příznaků a po plném rozvinutí typických potíží se v další vlně mohou objevit příznaky zdánlivě velmi vzdálené. Léčba neurodegenerativních chorob Používají se různé léky a některé další typy biologické léčby, své místo má psychoterapie, socioterapie, rehabilitace a léčení přídatných onemocnění. Podle schématu rozvoje těchto onemocnění (tab. 1) je teoreticky možné ovlivnit léčbou každou fázi patogenetického řetězce. Ideální by byla terapie, která by zasáhla příčiny degenerativního procesu, tedy úroveň biochemickou, a především genetickou. Takovému přístupu se blíží léčba antisense drugs (bránící syntéze patologické bílkoviny), ale především terapie genová. Podívejme se, jaké dnes máme možnosti léčby. n Ovlivnění funkce určitých neuronů. Neurony navzájem komunikují prostřednictvím neurotransmiterů (Vesmír 75, 65, 150, 191, 255, 334, 1996/2–6, 75, 485, 1996/9) a degenerace nervových buněk se projeví jejich nedostatkem (může chybět jeden neurotransmiter, ale i více), což již vede k rozvoji příznaků. Na samém začátku Alzheimerovy demence především klesne aktivita acetylcholinu, což se později projeví poruchami paměti a úbytkem rozumových funkcí. Pohybové poruchy u Parkinsonovy nemoci zase souvisejí s poklesem počtu neuronů produkujících neurotransmiter dopamin (viz Vesmír 74, 65, 1995/2). Neurotransmitery jsou poměrně dobře přístupné farmakologické léčbě. Nedostatečné množství neurotransmiteru lze doplnit, buď ho lze dodat přímo, nebo je možné dodat jeho prekurzor, ze kterého se neurotransmiter v buňce syntetizuje. Také lze blokovat enzymy, které přenašeč odbourávají. Další strategií je podávání látek, které přímo aktivují přenašečové receptory (místa, na která se neuropřenašeče vážou). Navíc je možné ovlivnit celý přenašečový systém nepřímo, jiným přenašečovým systémem. Léčba založená na ovlivnění aktivity neurotransmiterů prodělala v posledním půlstoletí bouřlivý rozvoj, je úspěšná např. u Parkinsonovy choroby a nyní částečně i u Alzheimerovy demence. n Nespecifické zlepšení látkové výměny neuronů. Dnes máme k dispozici skupinu léčiv, která v neuronech zlepšují výměnu látek, zejména glukózy. Používá se např. piracetam, piritinol či extrakt z jinanu dvoulaločného (Ginkgo biloba). Léčí se jimi organicky podmíněné poruchy nervového systému včetně degenerativních stavů. Problémem zůstává poměrně malá účinnost těchto léků, postup nemoci mohou jen zpomalit, výjimečně takřka zastavit. Dalším způsobem léčby je ovlivnění kalciových kanálů. Jejich činnost (otevření a zavření) závisí na elektrickém potenciálu neuronální membrány. Je-li průnik vápníku do neuronu nadměrný, vede to k zániku neuronu. Dnes máme k dispozici léky (nimodipin, flunarizin), které kalciové kanály „zavřou“ a tím degeneraci zpomalí. Degenerativní proces mohou zpomalit také léky omezující vliv volných kyslíkových radikálů. Tyto radikály jsou chemicky vysoce účinné a nepříznivě ovlivňují mnoho článků v řetězci látkové výměny. Vitaminy E a C, ale i některé další léky mohou nadbytečné volné kyslíkové radikály vychytat. U mnoha degenerativních onemocnění byl zjištěn nedostatek nervových růstových faktorů. Dnes se pokusně zavádějí stimulátory růstu nervové tkáně, které obsahují růstové faktory. Jedním z řešení je také neurochirurgická léčba, při které se do mozku nemocných lidí zavádějí štěpy embryonální tkáně. Smyslem je doplnit nejen chybějící nervové růstové faktory, ale i chybějící neurotransmitery. Tato léčba se dnes uplatňuje především při transplantaci embryonálních buněk substantia nigra u Parkinsonovy nemoci. Transkripci patologických proteinů způsobené mutací by mohly zabránit již zmíněné antisense drugs. Vlákno m-RNA přenáší genetickou informaci z jádra V síti... Možná to bude znít trochu podivně, ale anatomie pro mne byla vždy vědou jaksi sběratelskou. Přestože anatomové vlastně nic nesbírají, jejich věda má v sobě cosi z vášně skutečných sběratelů. Snaží se objekty svého výzkumu rozkouskovat na co nejmenší částečky, roztřídit je a každou důkladně popsat a pojmenovat, a popsat a pojmenovat i každý výstupek, důleček i každou odchylku v čase a prostoru. Oni vlastně ti anatomové sběrateli jsou – sbírají informace. Plnou měrou to potvrzuje i internet. Málokteré odvětví má již dnes tak obsáhlé, propracované a pečlivě utříděné www stránky, jako právě anatomie. A je jich po světě mnoho. Zaměřím se dnes jen na ty neuroanatomické. Jeden z nejlepších anatomických atlasů mozku najdete na stránce The whole brain atlas na adrese http:/ buněk do ribozomů, v nichž probíhá syntéza bílkovin. Antisense drugs jsou komplementární oligonukleotidy, které se prostřednictvím dusíkatých bází navážou na konkrétní m-RNA. Tím zabrání syntéze patologické bílkoviny, a tedy i rozvoji nemoci. Antisense drugs by mohly být vhodné pro léčbu Alzheimerovy nemoci. Problémem zatím zůstává obtížná příprava těchto farmak a transport léčiva do cílové tkáně. Navzdory intenzivnímu výzkumu nejsou antisense drugs dosud k dispozici v léčbě. Požadavek léčit příčinu choroby splňuje až genová terapie. Je-li nemoc způsobena nefunkční nebo chybějící bílkovinou, je teoreticky možné dodat tělu genetický materiál pro její tvorbu – buď holou DNA, nebo úsek DNA navázaný na nosič (vektor). Tím je většinou geneticky upravený vir. Komplexní přístup představuje implantace umělé geneticky naprogramované tkáně (neoorgánu), která by syntetizovala požadovanou bílkovinu. V současnosti probíhá výzkum genové terapie Alzheimerovy demence a Parkinsonovy choroby. Antisense drugs a genová terapie by se v některých indikacích mohly kombinovat. V posledním desetiletí výzkum neurodegenerativních chorob zaznamenal výrazný pokrok. Genetické a biologické modely těchto chorob představují nové možnosti terapie a prevence. Dosavadní léčba byla založena na regulaci neurotransmiterů a nespecifickém zlepšení metabolizmu neuronů. Na obzoru jsou však léčebné postupy, které by již mohly postihovat samotnou podstatu těchto vážných chorob. LITERATURA Hardy J., Gwin-Hardy K.: Genetic classification of primary neurodegenerative disease, Science 282, 1075–1079, 1998 Shoulson I.: Experimental therapeutics of neurodegenerative disorders: unmet needs, Science 282, 1072–1074, 1998 Valchář M.: Genetika a nemoci CNS, Psychiatrie 4, 223–237, 1998 Článek doplňuje tabulka v rubrice Data a souvislosti na s. 330. /www.med.har vard.edu/AANLIB/home.html. Obsahuje obrovské množství snímků zdravého mozku a všech jeho struktur i mozku s patologickými změnami při různých chorobách. Jsou přehledně zpřístupněny jakýmsi obrazovým navigátorem, vlastně „šoupátkem“, kterým lze nastavit polohu řezu, jenž chcete vidět. Většina řezů je nasnímána několika zobrazovacími technikami a je také možné zobrazit nebo skrýt ukazovátka a popisky jednotlivých struktur (viz obr.). Komu by to ještě nestačilo, pro toho jsou připraveny animace a applety naprogramované v javě, kdy se z prohlížeče stává téměř plnohodnotný program, jakým bývají opatřeny encyklopedie, slovníky a atlasy vydávané na CD-ROM. Další kvalitní neuroanatomický atlas sídlí na http:/ /www.neuropat.dote.hu/atlas.html. Těm, kteří touží spíš po textových informacích než po obrázcích, bych doporučil http://web.indstate.edu/thcme/anderson/ disease.html. Historii neurověd mapuje stránka http://www.soton.ac.uk/~jrc3/chudler/hist.html. A ještě jako doplňující informaci – obsáhlá sbírka odkazů na stránky pojednávající o neuroanatomii je na http://www.neuropat.dote.hu/. pH http://www.cts.cuni.cz/vesmir l VESMÍR 78, červen 1999 309
Podobné dokumenty
Blok 1 - Conference Partners Prague
 časné pády a supranukleární atrofie mesencefala a
okohybné poruchy
inkluse v ncl. caudatus
Song et al. Clinical correlates of similar pathologies in
parkinsonian syndromes. Mov Disord 2011;26:499-506
časné pády a supranukleární atrofie mesencefala a
okohybné poruchy
inkluse v ncl. caudatus
Song et al. Clinical correlates of similar pathologies in
parkinsonian syndromes. Mov Disord 2011;26:499-506
Je toho až nad hlavu!
 Neurověda se zabývá výzkumem
mozku a nervového systému,
jeho stavbou, funkcí a poruchami.
Neurověda se jako vědecká disciplína
rozvinula v posledních několika
desetiletích.
Lidský mozek je, jak neu...
Neurověda se zabývá výzkumem
mozku a nervového systému,
jeho stavbou, funkcí a poruchami.
Neurověda se jako vědecká disciplína
rozvinula v posledních několika
desetiletích.
Lidský mozek je, jak neu...
HCH minimografie *, 279 kB
 tendenci k agregaci. Agregáty a inkluze
se hromadí nejen v cytoplazmě, ale i v jádrech neuronů (obr. 3).
Význam agregátů huntingtinu není
ještě jednoznačně interpretován – je
možné, že agregáty nej...
tendenci k agregaci. Agregáty a inkluze
se hromadí nejen v cytoplazmě, ale i v jádrech neuronů (obr. 3).
Význam agregátů huntingtinu není
ještě jednoznačně interpretován – je
možné, že agregáty nej...
Morfologie mozku u schizofrenie: nálezy, metody a otázky
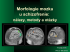 B: Hodnocení in vivo – zobrazovací metody
C: Nálezy u schizofrenie
D: Vybrané otázky
– Progrese
– Vliv antipsychotik
– MRI a klinika
E: CZEBRIC/CEBRIC
B: Hodnocení in vivo – zobrazovací metody
C: Nálezy u schizofrenie
D: Vybrané otázky
– Progrese
– Vliv antipsychotik
– MRI a klinika
E: CZEBRIC/CEBRIC
Nemoci s Lewyho tělísky
 diagnózou Parkinsonovy nemoci. Usoudil tedy, že nemají
v patofyziologii nemoci zásadní význam.
Naposledy se o tělíscích zmínil v roce 1924 v stručné příručce
o Parkinsonově nemoci, kde napsal:
„Nic...
diagnózou Parkinsonovy nemoci. Usoudil tedy, že nemají
v patofyziologii nemoci zásadní význam.
Naposledy se o tělíscích zmínil v roce 1924 v stručné příručce
o Parkinsonově nemoci, kde napsal:
„Nic...
Zpravodaj Archa č. 43 *, 4160 kB
 Celý náš život je angažovaností do záležitostí, které nás nad
chnou, znechutí, posilují nebo vyčerpávají. To, že býváme vtaženi do děje a jsme zapojeni emotivně, tělesně duševně nebo duchovně nás...
Celý náš život je angažovaností do záležitostí, které nás nad
chnou, znechutí, posilují nebo vyčerpávají. To, že býváme vtaženi do děje a jsme zapojeni emotivně, tělesně duševně nebo duchovně nás...



