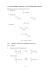Full text
Transkript
COMPARISON OF METALLIC ALLOYS CONTAINING ALUMINIUM FOR THE REDUCTIVE DEHALOGENATION OF AROMATIC COMPOUNDS SROVNÁNÍ KOVOVÝCH SLITIN S OBSAHEM HLINÍKU NA CHEMICKOU DEGRADACI HALOGENOVANÝCH AROMATICKÝCH SLOUČENIN Tomáš Weidlich1), Lubomír Prokeš2) 1) University of Pardubice, Faculty of Chemical Technology, Institute of Environmental and Chemical Engineering, Chemical Technology Group, Studentská 573, 532 10 Pardubice, Czech Republic, e-mail: [email protected] 2) Masaryk University, Faculty of Science, Department of Chemistry, Kamenice 753/5, 625 00 Brno, Czech Republic, e-mail: [email protected] Abstract: The comparison of different types of powdered metalic alloys with aluminium content was made for the reductive dehalogenation of polar halogenoaromatics (halogenated anilines, halogenated benzoic acids and phenols) in alkaline aqueous solution. The aluminium alloys with higher copper or nickel content enable effective dehalogenation of halogenoaromatics. The halogenoaromatics were completely converted to the appropriatte aromatics after less than one hour at room temperature using vigorous stirring. Keywords: Halogenated anilines, halogenated phenols, halogenated benzoic acids, aluminium alloy Abstrakt: V práci jsou shrnuty výsledky experimentálního ověřování hliníkových slitin v práškové formě na dehalogenaci polárních aromatických halogenderivátů, jakými jsou halogenované aniliny, benzoové kyseliny a fenoly, v alkalickém vodném roztoku. Použití hliníkových slitin s obsahem mědi nebo niklu umožňuje úplnou dehalogenaci uvedených halogenderivátů během desítek minut působení za laboratorní teploty za podmínek účinného míchání. Klíčová slova: Halogenované aniliny, halogenované fenoly, halogenované benzoové kyseliny, hliníkové slitiny Úvod Halogenované aromatické sloučeniny jsou do životního prostředí emitovány ve značných množstvích při výrobě a aplikaci chemických specialit, jakými jsou pesticidy, léčiva, aditiva do plastů a barviva a pigmenty (Tarawneh et al.). I přesto, že působí toxicky, se tyto látky dostávají do životního prostředí ve velkém množství, protože jsou součástí herbicidů (např. Dicamba, MCPA, Monuron, Chlorotoluron, Diuron atd.), biocidních přípravků pro úpravu dřeva, nátěrů a přírodních vláken (pentachlorfenol, tribromfenol) nebo meziprodukty běžně užívaných pesticidů, léčiv nebo barviv. Halogenované aniliny, fenoly a benzoové kyseliny v přírodě dále vznikají jako produkty biodegradace výše uvedených účinných látek (Field and Alvarez, Monferran et al., Rieger et al., Nagaoka et al.). Třeba 2,4,6-tribromfenol (TBF) je ve světě nejmasověji vyráběný bromovaný fenol. Jeho světová produkce v roce 2001 dosahovala hodnoty 9500 tun a předpokládá se její další nárůst (Howe). TBF se používá především jako meziprodukt při výrobě zpomalovačů hoření (tribromfenyl-allyl etheru a 1,2-bis(2,4,6-tribromophenoxy)-ethanu používaných pro modifikaci délky polymerních řetězců bromovaných epoxidových pryskyřic vyráběných z tetrabrombisfenolu A) pro výrobce elektroniky (plastové díly televizorů, počítačů a další domácí elektroniky). TBF se dále používá jako biocidní prostředek na ochranu dřeva, kde nahrazuje dříve hojně užívaný, ale toxičtější a hůře biologicky odbouratelný pentachlorfenol (při aplikacích užívaný ve formě sodné soli, Howe). TBF se dále tvoří ve značných množstvích během pyrolýzy tetrabromobisfenolu A (Barontini et al.). Halogenované aniliny, benzoové kyseliny i fenoly se mohou díky své značné rozpustnosti ve vodě (rozpustnost při 25 oC 4-chlorbenzoové kyseliny je 0,1 g/l, 3-chlorbenzoové kyseliny je 0,4 g/l, 2-chlorbenzoové kyseliny 2,1 g/l, Yalkowsky and He) vyskytovat především v odpadních vodách vznikajících při výrobě a aplikaci výše zmiňovaných biocidních prostředků. Proto byla ověřována řada metod, které by bylo možné použít pro odstraňování ve vodě rozpuštěných halogenovaných aromatických sloučenin. Mezi hlavní reprezentanty těchto metod patří chemická oxidace s použitím UV záření (obvykle za katalýzy TiO2, Enriquez et al., Chen and Dionysiou, Rosenfeldt and Linden), Fentonova oxidace (Benitez et al., Katsoyiannis et al.), ozonizace (BenoitGuyod et al., Huang et al., Azrague et al., Li et al.), elektrochemická oxidace (Kishimoto et al., Zaror et al., J. Kim and Korshin), působení γ-záření (Zona et al., Bojanowska-Czajka et al.). Hlavním problémem všech těchto metod je, že během oxidace sice dochází k rozkladu halogenovaných aromatických sloučenin, ale vznikají při něm jiné halogenované aromatické deriváty, jako např. halogensalicylové kyseliny, halogenované fenoly a chlorbenzen, jak dokumentuje obr. 1. Za podmínek dostatečně dlouhé doby chemické oxidace a velkých přebytků oxidačních činidel dochází k rozkladu těchto zmiňovaných meziproduktů až na oxid uhličitý, vodu a halogenovodíky (Li et al.). Naproti tomu reduktivní dehalogenace halogenovaných aromatických sloučenin probíhá relativně selektivně, přičemž nejprve dochází k náhradě halogenů vázaných na aromatické jádro vodíkem či jiným substituentem, za vzniku příslušné aromatické sloučeniny, jejíž toxicita je ve srovnání s výchozí halogenovanou aromatickou sloučeninou obvykle nižší a navíc se výrazně zlepšuje biodegradovatelnost produktů dehalogenace. Existuje několik přístupů k provedení reduktivní dehalogenace, jsou známy katalytické hydrodehalogenace aromatických halogenderivátů, ty však vyžadují práci za zvýšeného tlaku a teploty v přítomnosti plynného vodíku a drahých kovů jako katalyzátorů (Aramendıa et al.). Jinou ekonomicky zajímavou možností pro degradaci halogenovaných organických sloučenin je reduktivní dehalogenace s použitím neušlechtilých kovů, mezi nejpoužívanější patří Al, Fe, Zn, Mg (Contreras et al.), protože patří mezi nejméně toxické či jinak nebezpečné, pro tento účel použitelné kovy (Alonso et al., Tashiro and Fukata, Liu et al., Lee et al., Akagah et al.). Zvláště hliník patří mezi nejúčinnější dehalogenační činidla pro odbourávání alifatických halogenderivátů (Alonso et al.). Zvýšenou reaktivitu hliník vykazuje především za podmínek, je-li použit ve formě slitin s kovy užívanými jako hydrogenační katalyzátory (Massicot et al., Lunn and Sansone, Yang et al., Liu et al.). Jednou z nejlepších slitin použitelných pro redukce je tzv. Raneyova slitina hliníku s niklem, která byla jinými autory použita pro dehalogenace chlorovaných bifenylů a tetrabromobisfenolu A (Lunn and Sansone, Liu et al.). Metodika Dehalogenační reakce byly prováděny s použitím 250ml kulatých baněk opatřených elektromagnetickým mícháním s použitím Starfish nástavce pro provádění reakcí za stejných podmínek současně v pěti reakčních baňkách. Hrdla baněk byla připojena na adsorpci plněnou granulovaným aktivním uhlím. Reakce probíhaly při temperaci na 25 oC. Do míchaných reakčních baněk na Starfish nástavci byla předložena odpovídající množství halogenovaných aromatických sloučenin a vodného NaOH (100 ml) a následně bylo do vzniklého roztoku přidáno odpovídající množství práškového kovu nebo kovové slitiny (podrobnosti jsou uvedeny v tabulkách). Reakční směsi byly míchány při 500 ot.-1 přes noc, následně byly z reakční směsi odebrány vzorky, které byly po filtraci analyzovány na obsah rozpuštěných kovů s pomocí ICP-OES. Vzorky filtrátů při použití hliníku či slitin hliníku obsahovaly typicky 430-475 mg/l Al a cca 0.1 mg/l Ni. Pro identifikaci vznikajících produktů byly vzorky reakční směsi (25 ml vzorku) okyseleny na pH ~ 2 s 16% kyselinou sírovou a okyselená vodná vrstva byla opakovaně extrahována do deuterovaného chloroformu (1×0.5 ml a 2×0.5 ml). Chloroformový extrakt byl následně analyzován s pomocí 1 H NMR a GC-MS (Maniara et al., Ríos et al.). Po úpravě pH reakční směsi na hodnotu pH = 6,7 až 7,0 dochází k vylučování hydroxidů rozpuštěných kovů. Po oddělení těchto hydroxidů kovů filtrací klesne obsah kovů ve filtrátech na 0,05 mg/l Al a méně než 0,01 mg/l Ni (Weidlich et al.). Obr. 1: Chemická oxidace 4-chlorbenzoové kyseliny v modelové odpadní vodě (Li et al.). Výsledky Srovnání použití různých kovů a kovových slitin na dehalogenaci vybraných aromatických halogenderivátů uvádějí tabulky. V tabulce 1 jsou srovnávány výsledky redukce halogenovaných anilinů s použitím řady práškových kovů a jejich slitin, v tabulce 2 jsou shrnuty dosažené výsledky při aplikaci hliníku a hliníkových slitin na dehalogenaci 2-brom- a 2-chlorbenzoové kyseliny a na dechloraci 3,4-dichlorbenzoové kyseliny, v tabulce 3 jsou uvedeny výsledky experimentů při debromaci 2,4,6-tribromfenolu. Tab. 1: Výtěžek dehalogenace s použitím práškových kovů a slitin u studovaných halogenanilinů (XANs). Reakční podmínky:25oC/17 h míchání 10mM roztoků XAN v 1% vodném NaOH: Cl Exp. 1 2 3 4 5 6 7 Redukční činidlo (praškové) Al (2 g) Zn (2 g) Fe3Al (2 g) mosaz Cu-Zn (2 g) bronz Cu-Sn (2 g) Devardova sl. Al-Cu-Zn (2 g) Raneyova sl. Al-Ni (1 g) Br NH2 Cl NH2 NH2 0% 0% 0% <2% 0% 0% 0% 0% 0% 0% 0% 0% 0% 0% 0% 100 % 2-5 % 100 % 100 % 100 % 100 % Diskuse Při srovnání aplikace neušlechtilých kovů a jejich slitin s mědí či niklem je z uvedených tabulek zřejmé, že práškový hliník je výrazně méně účinné redukční činidlo než slitiny hliníku s mědí či niklem. Zajímavým poznatkem při aplikaci slitiny hliníku s mědí a zinkem (Devardovy slitiny) je pozorovaná selektivita redukce aromatických halogenderivátů, která nemá praktický význam pro procesy sanace, ale mohla by být zajímavá např. v organické technologii. Raneyova slitina hliníku s niklem je ve všech testovaných případech velmi účinné dehalogenační činidlo, které je schopné dehalogenovat všechny testované halogenderiváty se 100 konverzí na příslušné aromatické sloučeniny. Tab. 2: Dehalogenace halogenbenzoových kyselin (10mM roztok) v 1%ním NaOH s použitím uvedených kovů či kovových slitin Použité redukční činidlo: Konverze na Konverze na benzoovou kyselinu benzoovou kyselinu Br Konverze na benzoovou kyselinu Cl COOH Cl COOH Cl Al (10x mol. přebytek) 5% < 1% 0% Zn (10x mol. přebytek) 4.2 % < 1% 0% Al-Ni (2x mol. přebytek) 100% 100% 100% Al-Cu-Zn 100% 10,7% 0% * (10x mol. přebytek) * vzniká směs 3,4-dichlorbenzoové a 3-chlorbenzoové kyseliny v molárním poměru 1:1 COOH Tab. 3: Vliv různých redukčních činidel na debromaci 2,4,6-tribromfenolu (TBF)a Exp. NaOH (ekv.) Redukční činidlo (ekv. Al) Složení reakční směsi po reakci (mol. %)b Br Br OH OH OH Br Br 1 2 3 60 60 60 OH OH Br Br Br Al (10) 81 4.1 4.9 duralc (10) 0 15.1 0 Devardova 0 0 0 sl.(10) 4 60 Fe3Al (10) 99.2 0 0.8 5 60 mosaze 100 0 0 (15, Zn) 6 60 Zn (15, 0 63.4 20.4 Zn) 7 60 Mg (15, 99.3 0 0 Mg) 8 60 Fe (15, 100 0 0 Fe) 9 60 Al-Ni (10) 0 0 0 a tribromfenol (1 mmol, 0.33 g) v 100 ml dest. vody, 16h míchání za lab. t. b dle 1H NMR c dural AA2024 obsahuje 4,4% Cu, 1,5% Mg, 0,6% Mn a 93,5% Al d místo 2-bromfenolu v r.s. nalezen 4-bromfenol e obsahuje 70% Cu a 30% Zn Br 0 75.6 0 0 9.3 100 0 0 0 0 16.3 0 0.7d 0 0 0 0 100 Závěr Slitiny hliníku s mědí nebo niklem jsou v alkalickém vodném prostředí výrazně účinnější dehalogenační činidla než práškový hliník či jiné neušlechtilé kovy (hořčík, zinek, železo), přičemž k dehalogenaci dochází i za laboratorní teploty s použitím malého přebytku redukčního činidla oproti stechiometrii. Poděkování Příspěvek vznikl díky finanční pomoci Technologické agentury České Republiky (TA01010606). Literatura: Akagah A., J. C. Poite, M. Chanon, Reactive aluminum powders for the reduction of haloarenes. Application of the experiment-planning method for the optimization of obtaining reactive metal powder. Org. Prep. Proc. Int. 17 (1985), 219-23. Alonso F., I. P. Beletskaya, M. Yus, Metal-Mediated Reductive Hydrodehalogenation of Organic Halides. Chem. Rev. 102 (2002) 4009-4091. Aramendia M. A., V. Borau, M. Garcıa, C. Jimenez, J. M. Marinas, and F. J. Urbano. Liquid-phase hydrohalogenation of substituted chlorobenzenes over palladium supported catalysts. Appl. Catal. (2003), B.43:71–79. Azrague K., S. W. Osterhus, J. G. Biomorgi: Degradation of pCBA by catalytic ozonation in natural water. Water Sci. Technol. (2009), 59(6), 1209-1217. Barontini F., K. Marsanich, L. Petarca, V. Cozzani, The Thermal Degradation Process of Tetrabromobisphenol A. Ind. Eng. Chem. Res. 43 (2004) 1952-1961. Benitez F. J., Real F. J., Real J., Acero J. L., Garcia C., Llanos E. M.: Kinetics of phenylurea herbicides oxidation by Fenton and photo-Fenton processes. J. Chem. Technol. Biotechnol. (2007), 82(1), 65-73. Benoit-Guyod J. L., Crosby D. G., Bowers J. B.: Degradation of MCPA by ozone and light. Water Res. (1986), 20(1), 67-72. Bojanowska-Czajka A., P. Drzewicz, C. Kozyra, G. Nalecz-Jawecki, J. Sawicki, B. Szostek, M. Trojanowicz,: Radiolytic degradation of herbicide 4-chloro-2-methyl phenoxyacetic acid (MCPA) by γ-radiation for environmental protection.. Ecotoxicology and Environmental Safety (2006), 65(2), 265-277. Chen Y., D. D. Dionysiou: Correlation of structural properties and film thickness to photocatalytic activity of thick TiO2 films coated on stainless steel. Appl. Catal. B:Environmental (2006), 69(1-2), 24-33. Contreras D., C. Oviedo, R. Valenzuela, J. Freer, K. Rojo, J. Rodríguez, Tribromophenol degradation by a catechol-driven Fenton reaction, J. Chil. Chem. Soc. 54 (2009) 141-143. Enriquez R., A. G. Alexander, P. Pichat: Probing multiple effects of TiO2 sintering temperature on photocatalytic activity in water by use of a series of organic pollutant molecules. Catalysis Today (2007), 120(2), 196-202. Field J. A., R. S. Alvarez. Microbial transformation of chlorinated benzoates. Rev. Environ. Sci. Biotechnol. (2008), 7, 191–210. Howe P., S. Dobson, H. Malcolm, United Nations Environment Programme, World Health Organization, International Labour Organisation, Inter-Organization Programme for the Sound Management of Chemicals, International Program on Chemical Safety, ISBN:92 4 153066 9, ISSN:1020-6167; World Health Organization, Geneva 2005. Huang R. H., J. Liu, L. S. Li, Zhang, Z. Qiu Yun; X. Li; P. Lu: Fe/MCM-41 as a promising heterogeneous catalyst for ozonation of p-chlorobenzoic acid in aqueous solution. Chin. Chem. Lett. (2011), 22(6), 683-686. Katsoyiannis I. A., S. Canonica, U. von Gunten: Efficiency and energy requirements for the transformation of organic micropollutants by ozone, O3/H2O2 and UV/H2O2. Water Res. (2011), 45(13), 3811-3822. Kim J., G. V. Korshin: Examination of in situ Generation of Hydroxyl Radicals and Ozone in a Flowthrough Electrochemical Reactor. Ozone: Sci. Eng. (2008), 30(2), 113-119. Kishimoto N., Y. Morita, H. Tsuno, T. Oomura, H. Mizutani: Advanced oxidation effect of ozonation combined with electrolysis. Water Res. (2005), 39(19), 4661-4672. Lee C.-L., C.-J. G. Jou, H. P. Wang, Enhanced Degradation of Chlorobenzene in Aqueous Solution Using Microwave-Induced Zero-Valent Iron and Copper Particles. Water Environ. Res. (2010) 82(7), 642-646. Li X., Zhang, T. Qiuyun; L. Lili; S. Ping; F. Sun, L. Li:Catalytic ozonation of p-chlorobenzoic acid by activated carbon and nickel supported activated carbon prepared from petroleum coke. J. Hazard. Mater. (2009), 163(1), 115-120. Liu G.-B., H-Y. Zhao, T. Thiemann, Zn dust mediated reductive degradation of tetrabromobisphenol A (TBBPA). J. Hazard. Mater. 2009, 169, 1150-1153. Liu G.-B., M. Tashiro, T. Thiemann, A Facile Method for the Dechlorination of Mono- and Dichlorobiphenyls using Raney Ni-Al Alloy in Dilute Aqueous Solutions of Alkali Hydroxides or Alkali Metal Carbonates, Tetrahedron 65 (2009) 2497-2505. Liu G.-B., H.-Y. Zhao, J. Zhang, T. Thiemann, Raney Ni-Al alloy mediated hydrodehalogenation and aromatic ring hydrogenation of halogenated phenols in aqueous medium. J. Chem. Res. 6 (2009) 342-344. Lunn G., E. B. Sansone, Validated Methods for Degrading Hazardous Chemicals: Some Halogenated Compounds, AIHA Journal 52 (1991) 252-257. Maniara G., K. Rajamoorthi, S. Rajan, G. W. Stockton, Method performance and validation for quantitative analysis by 1H and 31P NMR spectroscopy. Applications to analytical standards and agricultural chemicals. Anal. Chem. 70 (1998) 4921. Massicot F., R. Schneider, Y. Fort, S. Illy-Cherrey, O. Tillement, Synergistic Effect in Bimetallic NiAl Clusters. Application to Efficient Catalytic Reductive Dehalogenation of Polychlorinated Arenes. Tetrahedron 56 (2000) 4765-4768. Monferran V. M., J. R. Echenique, D. A. Wunderlin: Degradation of chlorobenzenes by a strain of Acidovorax avenae isolated from a polluted aquifer. Chemosphere (2005), 61, 98–106. Nagaoka T., J. Tanaka, K. Kouno, S. Yoshida, H. Tanaka, T. Ando: Generation of chlorinated aromatic acids during sludge-composting and their fate in soils. Soil Science and Plant Nutrition. (2001), 47(3), 443-453. Rieger P. G., H. M. Meier, M. Gerle, U. Vogt, T. Growth, and H. J. Knackmuss. Xenobiotics in the environment: Present and future strategies to obviate the problem of biological persistence. J. Biotechnol. (2002), 94, 101–123. Ríos S. M., C. M. Barquín, C. N. Nudelman, Hydrocarbons characterization in coastal sediments of the Argentine Patagonia using the nuclear magnetic resonance (NMR) spectroscopy . Environ. Chem. Lett. 8, (2010) 223-229. Rosenfeldt E. J., K. G. Linden: The ROH,UV Concept to Characterize and the Model UV/H2O2 Process in Natural Waters. Environ. Sci. Technol. (2007), 41, 2548-2553. Tarawneh K. A., F. Irshaid, I. H. Ajlundi, M. M. Abboud,N. A. Mohammed,A. M. Khleifat: Biodegradation Kinetics of Four Substituted Chlorobenzoic Acids by Enterobacter aerogenes. Bioremediation J., (2010), 14(2) 55–66. Tashiro M., G. Fukata, Studies on selective preparation of aromatic compounds. XII. The selective reductive dehalogenation of some halophenols with zinc powder in basic and acidic media. J. Org. Chem. 42 (1977) 835-838. Weidlich T., A. Krejcova, L. Prokes: Study of dehalogenation of halogenoanilines using Raney Al–Ni alloy in aqueous medium at room temperature. Monatsh. Chem. 141 (2010) 1015–1020. Weidlich T., L.Prokes: Facile dehalogenation of halogenated anilines and their derivatives using Al-Ni alloy in alkaline aqueous solution. Cent. Eur. J. Chem. 9 (2011) 590-597. Yalkowsky S. H., Y. He: Handbook of Aqueous Solubility Data. CRC Press, London, 2003, p.350. Yang B., S. Deng, G. Yu, H. Zhang, J. Wu, Q. Zhuo, Bimetallic Pd/Al particles for highly efficient hydrodechlorination of 2-chlorobiphenyl in acidic aqueous solution. J. Hazard. Mater. 189 (2011) 7683. Zaror C. A., C. Salazar, E. A. Araneda, M. A. Mondaca, H. D. Mansilla, C. Pena: Electrochemical treatment of segregated effluents from the D-stage in ECF kraft cellulose bleaching. J. Adv. Oxidation Technol. (2011), 14(1), 47-53. Zona R., S. Solar, N. Getoff, K. Sehested, J. Holcman: Reactivity of OH radicals with chlorobenzoic acids-A pulse radiolysis and steady-state radiolysis study. Radiation Phys. Chem. (2010), 79(5), 626636.
Podobné dokumenty
Molekulární modelování a vlastnosti epoxidových pryskyřic
 některé jevy na povrchu uhlíkových a dalších textilních vláken [10-13]. V tomto příspěvku
chceme ukázat možnosti molekulárního modelování pro odhady vlastností pryskyřic, tvrdidel,
reaktivních ředi...
některé jevy na povrchu uhlíkových a dalších textilních vláken [10-13]. V tomto příspěvku
chceme ukázat možnosti molekulárního modelování pro odhady vlastností pryskyřic, tvrdidel,
reaktivních ředi...
1. 1. 2009, 00:16
 PC navzájem udělili; k 12/2 1999 jich bylo přesně 37). Celou radu mrzí, že zásadní programové
prohlášení rady5, které bylo doporučeno k přijetí i IUPACem, zůstalo poněkud ve stínu předchozích
infor...
PC navzájem udělili; k 12/2 1999 jich bylo přesně 37). Celou radu mrzí, že zásadní programové
prohlášení rady5, které bylo doporučeno k přijetí i IUPACem, zůstalo poněkud ve stínu předchozích
infor...
požadavky k přijímacím zkouškám v jednotlivých oborech pro
 Triády železa a platinových kovů; Prvky skupiny mědi a zinku: výroba kovů, fyzikální a chemické
vlastnosti prvků, sloučeniny, použití.
Organická chemie
Třídění organických sloučenin podle oxidačníc...
Triády železa a platinových kovů; Prvky skupiny mědi a zinku: výroba kovů, fyzikální a chemické
vlastnosti prvků, sloučeniny, použití.
Organická chemie
Třídění organických sloučenin podle oxidačníc...
Molekulární modelování - Výzkumné centrum TEXTIL II
 MM tři významné kroky:
a) Zahrnutí van der Waalsovských interakcí do silového pole (T. L. Hill).
b) Aplikace MM na výpočet poměru jednotlivých produktů v reakční směsi, vzniklé SN2
reakcí (I. Dostr...
MM tři významné kroky:
a) Zahrnutí van der Waalsovských interakcí do silového pole (T. L. Hill).
b) Aplikace MM na výpočet poměru jednotlivých produktů v reakční směsi, vzniklé SN2
reakcí (I. Dostr...
 Superpočítače bez uživatelů nemají žádné opodstatnění. Hlavním účelem této ročenky
je proto ukázat ne technické a programové vybavení, ale především prezentovat hlavní
úlohy, které se na počítačích...
Superpočítače bez uživatelů nemají žádné opodstatnění. Hlavním účelem této ročenky
je proto ukázat ne technické a programové vybavení, ale především prezentovat hlavní
úlohy, které se na počítačích...
SPOLUPRÁCE ROSTLIN A MIKROORGANISMŮ NA ODSTRANĚNÍ
 rostlin pěstovaných v půdě s přídavkem chlorbenzoových kyselin a také špatného vývoje květů u těchto
rostlin.
Závěr
Po půl roce došlo v půdě k úbytku všech testovaných chlorbenzoových kyselin z toh...
rostlin pěstovaných v půdě s přídavkem chlorbenzoových kyselin a také špatného vývoje květů u těchto
rostlin.
Závěr
Po půl roce došlo v půdě k úbytku všech testovaných chlorbenzoových kyselin z toh...
 SZANDAR-JAGOSZ Katarzyna
SZANDAR-JAGOSZ Katarzyna